Conegudes com a cèl·lules punyal pel seu acrònim en anglès, les STAb són la nova evolució de la immunoteràpia contra el càncer. En essència, són cèl·lules armades amb punyals moleculars que els permeten identificar i destruir cèl·lules tumorals i que, alhora, són capaces de repartir i distribuir aquestes armes a altres cèl·lules de defensa per fer extensiva la seva capacitat de reconeixement del càncer.
El disseny d’aquestes cèl·lules neix com una mena de perfeccionament de les cèl·lules CAR-T, que ja van suposar una revolució en la immunologia des del seu llançament el 2017 i demostra, un cop més, el potencial de la immunoteràpia en càncer i el ritme trepidant al qual avança. La investigació de les STAb i el seu desenvolupament ha estat liderat per un equip d’investigadors de l’Hospital Universitari 12 d’Octubre de Madrid, en col·laboració amb altres centres com l’Institut de Recerca contra la Leucèmia Josep Carreras.
Fa temps que hi treballen i cada cop estan més a prop d’aconseguir l’aplicació clínica de la teràpia amb STAb. L’article publicat a Science Translational Medicine el passat 14 de febrer és un pas més en aquesta direcció, i demostra el ventall de possibilitats que obre en el tractament del càncer, enfocant-se en el mieloma múltiple. En aquest cas, els investigadors han demostrat amb models experimentals que les STAb són molt més efectives que la teràpia per cèl·lules CAR-T que s’utilitzava, i que pot arribar a beneficiar a pacients que n’eren resistents i patien recaigudes importants.
Com funciona el CAR-T?
El mètode d’acció de les CAR-T es basa a dotar a l’organisme d’unes cèl·lules de defensa especialment dissenyades per atacar el càncer. Per aconseguir aquesta especificitat tumoral, normalment s’extreuen cèl·lules immunitàries del mateix pacient (o d’un donant) i es modifiquen genèticament per fer que tinguin per diana molècules típiques del tumor a tractar. Així, les CAR-T s’entendrien com a armes dirigides. La teràpia acaba sent totalment personalitzada, concreta pel tumor de cada pacient, i acostuma a tenir resultats força bons.
Ara bé, de vegades apareixen complicacions en què, entre altres, les mateixes defenses del pacient reaccionen contra les CAR-T o el tumor s’adapta a poc a poc a la nova situació i es torna resistent. Una de les estratègies d’escapament tumoral que s’han detectat, sobretot en mieloma múltiple, consisteix a bombardejar les CAR-T amb la seva pròpia diana. És a dir, el tumor passa a alliberar al medi la molècula per la qual és identificada per les CAR-T, de forma massiva, i així aconsegueix bloquejar-les i evitar que arribin a identificar-lo. En certa manera, es podria entendre que el tumor s’amaga darrere una allau de molècules que atabalen i mantenen ocupades a les CAR-T.
Aquest és precisament un dels problemes que les cèl·lules STAb han superat. Les cèl·lules STAb, a diferència de les CAR, no només poden veure el tumor sinó que també recluten a altres cèl·lules immunitàries (cèl·lules T) i les tornen capaces de fer-ho, engruixint les files de les defenses i amplificant notablement l’efecte anticancerós.
Com ho fan?
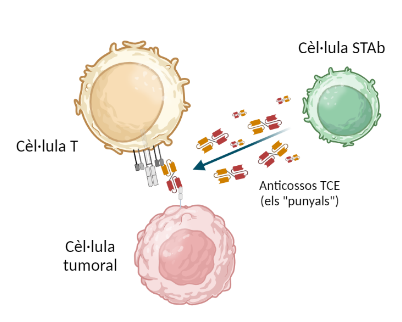
Això ho fan gràcies a la producció i alliberament d’anticossos TCE que tenen dos braços de reconeixement: amb un reconeixen un receptor típic de cèl·lules T i, amb l’altre, reconeixen molècules que estan exposades a la superfície del tumor. Les STAb alliberen grans quantitats
d’aquests anticossos, que s’enganxen a les cèl·lules T per un braç i permeten que aquestes identifiquin el tumor amb l’altre braç, s’activin i l’ataquin. Literalment, les STAb armen les cèl·lules T contra el càncer. Així, el fet d’augmentar enormement el nombre de cèl·lules capaces d’identificar i atacar específicament el tumor, fa que l’estratègia de bombardeig i distracció de les cèl·lules canceroses deixi de funcionar i, alhora, incrementa el potencial per destruir-lo.
A més, s’ha comprovat que les cèl·lules STAb generen una memòria immunològica més duradora que les CAR i, per tant, el seu efecte és encara més llarg. En conjunt, tot això fa que les STAb es presentin com una estratègia terapèutica més efectiva, que esquiva els mecanismes de resistència tumoral predominants i que aconsegueix resultats a dosis molt menors, abaratint costos de producció. És inevitable preveure una aplicació clínica d’aquesta teràpia en pacients en un futur pròxim, que suposaria una millora o complement a les cèl·lules CAR. Queda per veure com evolucionen els assajos clínics per a poder passar al món real i encaixar els punyals de les STAb en el panorama terapèutic actual.

