Conocidas como células puñal por su acrónimo en inglés, las STAb son la nueva evolución de la inmunoterapia contra el cáncer. En esencia, son células armadas con puñales moleculares que los permiten identificar y destruir células tumorales y que, a la vez, son capaces de repartir y distribuir estas armas a otras células de defensa para hacer extensiva su capacidad de reconocimiento del cáncer.
El diseño de estas células nace como un tipo de perfeccionamiento de las células CAR-T, que ya supusieron una revolución en la inmunología desde su lanzamiento el 2017 y demuestra, un golpe más, el potencial de la inmunoterapia en cáncer y el ritmo trepidante al cual avanza. La investigación de las STAb y su desarrollo ha sido liderado por un equipo de investigadores del Hospital Universitario 12 de Octubre de Madrid, en colaboración con otros centros como el Instituto de Investigación contra la Leucemia Josep Carreras.
Hace tiempo que trabajan y cada vez están más cerca de conseguir la aplicación clínica de la terapia con STAb. El artículo publicado a Science Translational Medicine el pasado 14 de febrero es un paso más en esta dirección, y demuestra el abanico de posibilidades que abre en el tratamiento del cáncer, enfocándose en el mieloma múltiple. En este caso, los investigadores han demostrado con modelos experimentales que las STAb son mucho más efectivas que la terapia por células CAR-T que se utilizaba, y que puede llegar a beneficiar a pacientes que eran resistentes y sufrían recaídas importantes.
¿Cómo funciona el CAR-T?
El método de acción de las CAR-T se basa en dotar al organismo de unas células de defensa especialmente diseñadas para atacar el cáncer. Para conseguir esta especificidad tumoral, normalmente se extraen células inmunitarias del mismo paciente (o de un donante) y se modifican genéticamente para hacer que tengan por diana moléculas típicas del tumor a tratar. Así, las CAR-T se entenderían como armas dirigidas. La terapia acaba siendo totalmente personalizada, concreta por el tumor de cada paciente, y acostumbra a tener resultados bastante buenos.
Ahora bien, a veces aparecen complicaciones en que, entre otras, las mismas defensas del paciente reaccionan contra las CAR-T o el tumor se adapta despacio a la nueva situación y se vuelve resistente. Una de las estrategias de escape tumoral que se han detectado, sobre todo en mieloma múltiple, consiste a bombardear las CAR-T con su propia diana. Es decir, el tumor pasa a liberar al medio la molécula por la cual es identificada por las CAR-T, de forma masiva, y así consigue bloquearlas y evitar que lleguen a identificarlo. En cierto modo, se podría entender que el tumor se esconde detrás una avalancha de moléculas que agobian y mantienen ocupadas a las CAR-T.
Este es precisamente uno de los problemas que las células STAb han superado. Las células STAb, a diferencia de las CAR, no solo pueden ver el tumor, sino que también reclutan a otras células inmunitarias (células T) y las vuelven capaces de hacerlo, agrandando las filas de las defensas y amplificando notablemente el efecto anticanceroso.
¿Cómo lo hacen?
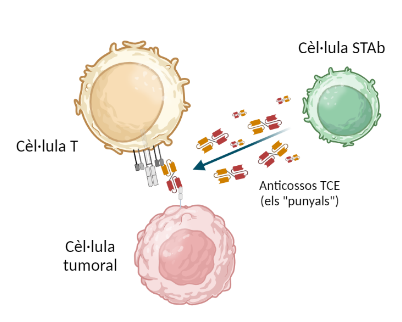
Esto lo hacen gracias a la producción y liberación de anticuerpos TCE que tienen dos brazos de reconocimiento: con uno reconocen un receptor típico de células T y, con el otro, reconocen moléculas que están expuestas a la superficie del tumor. Las STAb liberan grandes cantidades
de estos anticuerpos, que se enganchan a las células T por un brazo y permiten que estas identifiquen el tumor con el otro brazo, se activen y lo ataquen. Literalmente, las STAb arman las células T contra el cáncer. Así, el hecho de aumentar enormemente el número de células capaces de identificar y atacar específicamente el tumor, hace que la estrategia de bombardeo y distracción de las células cancerosas deje de funcionar y, a la vez, incrementa el potencial para destruirlo.
Además, se ha comprobado que las células STAb generan una memoria inmunológica más duradera que las CAR y, por lo tanto, su efecto es todavía más largo. En conjunto, todo esto hace que las STAb se presenten como una estrategia terapéutica más efectiva, que esquiva los mecanismos de resistencia tumoral predominantes y que consigue resultados a dosis muy menores, abaratando costes de producción. Es inevitable prever una aplicación clínica de esta terapia en pacientes en un futuro próximo, que supondría una mejora o complemento a las células CAR. Queda para ver como evolucionan los ensayos clínicos para poder pasar en el mundo real y encajar los puñales de las STAb en el panorama terapéutico actual.

